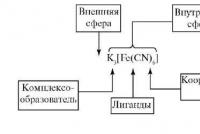
Костная ткань состоит из клеток. Костная ткань, общая характеристика
Костная ткань является разновидностью соединительной ткани и состоит из клеток и межклеточного вещества, в котором содержится большое количество минеральных солей, главным образом фосфат кальция. Минеральные вещества составляют 70 % от костной ткани, органические - 30 %.
Функции костных тканей:
Опорная;
Механическая;
Защитная;
Участие в минеральном обмене организма - депо кальция и фосфора.
Классификация костных тканей
Различают две разновидности костных тканей:
Ретикулофиброзную (грубоволокнистую);
Пластинчатую (параллельно волокнистую).
В ретикулофиброзной костной ткани пучки коллагеновых волокон толстые, извилистые и располагаются неупорядочено. В минерализованном межклеточном веществе в лакунах беспорядочно располагаются остеоциты. Пластинчатая костная ткань состоит из костных пластинок, в которых коллагеновые волокна или их пучки располагаются параллельно в каждой пластинке, но под прямым углом к ходу волокон в соседних пластинках. Между пластинками в лакунах располагаются остеоциты, тогда как их отростки проходят в канальцах через пластинки.
В организме человека костная ткань представлена почти исключительно пластинчатой формой. Ретикулофиброзная костная ткань встречается только как этап развития некоторых костей (теменных, лобных). У взрослых людей они находятся в области прикрепления сухожилий к костям, а также на месте окостеневших швов черепа (стреловидный шов чешуи лобной кости).
Клетки костной ткани: остеобласты, остеоциты, остеокласты. Основными клетками в сформированной костной ткани являются остеоциты. Это клетки отростчатой формы с крупным ядром и слабовыраженной цитоплазмой (клетки ядерного типа). Тела клеток локализуются в костных полостях - лакунах, а отростки - в костных канальцах. Многочисленные костные канальцы, анастомозируя между собой, пронизывают всю костную ткань, сообщаясь с периваскулярными пространствами, и образуют дренажную систему костной ткани. В этой дренажной системе содержится тканевая жидкость, посредством которой обеспечивается обмен веществ не только между клетками и тканевой жидкостью, но и межклеточным веществом. Для ультраструктурной организации остеоцитов характерно наличие в цитоплазме слабовыраженной зернистой эндоплазматической сети, небольшого числа митохондрий и лизосомы, центриоли отсутствуют. В ядре преобладает гетерохроматин. Все эти данные свидетельствуют о том, что остеоциты обладают незначительной функциональной активностью, которая заключается в поддержании обмена веществ между клетками и межклеточным веществом. Остеоциты являются дефинитивными формами клеток и не делятся. Образуются они из остеобластов.
Остеобласты содержатся только в развивающейся костной ткани. В сформированной костной ткани они отсутствуют, но содержатся обычно в неактивной форме в надкостнице. В развивающейся костной ткани они охватывают по периферии каждую костную пластинку, плотно прилегая друг к другу, образуя подобие эпителиального пласта. Форма таких активно функционирующих клеток может быть кубической, призматической, угловатой. В цитоплазме остеобластов содержится хорошо развитая зернистая эндоплазматическая сеть и пластинчатый комплекс Гольджи, много митохондрий. Такая ультраструктурная организация свидетельствует о том, что эти клетки являются синтезирующими и секретирующими. Действительно, остеобласты синтезируют белок коллаген и гликозоаминогликаны, которые затем выделяют в межклеточное пространство. За счет этих компонентов формируется органический матрикс костной ткани. Затем эти же клетки обеспечивают минерализацию межклеточного вещества посредством выделения солей кальция. Постепенно, выделяя межклеточное вещество, они как бы замуровываются и превращаются в остеоциты. При этом внутриклеточные органеллы в значительной степени редуцируются, синтетическая и секреторная активность снижается и сохраняется функциональная активность, свойственная остеоцитам. Остеобласты, локализующиеся в камбиальном слое надкостницы, находятся в неактивном состоянии, синтетические и транспортные органеллы слабо развиты. При раздражении этих клеток (в случае травм, переломов костей и так далее) в цитоплазме быстро развивается зернистая эндоплазматическая сеть и пластинчатый комплекс, происходит активный синтез и выделение коллагена и гликозоаминогликанов, формирование органического матрикса (костная мозоль), а затем и формирование дефинитивной костной ткани. Таким способом за счет деятельности остеобластов надкостницы, происходит регенерация костей при их повреждении.
Отеокласты - костеразрушающие клетки, в сформированной костной ткани отсутствуют. Но содержатся в надкостнице и в местах разрушения и перестройки костной ткани. Поскольку в онтогенезе непрерывно осуществляются локальные процессы перестройки костной ткани, то в этих местах обязательно присутствуют и остеокласты. В процессе эмбрионального остеогистогенеза эти клетки играют важную роль и определяются в большом количестве. Остеокласты имеют характерную морфологию: во-первых, эти клетки являются многоядерными (3-5 и более ядер), во-вторых, это довольно крупные клетки (диаметром около 90 мкм), в-третьих, они имеют характерную форму - клетка имеет овальную форму, но часть ее, прилежащая к костной ткани, является плоской. При этом, в плоской части выделяют две зоны:
Центральная часть - гофрированная содержит многочисленные складки и островки;
Периферическая (прозрачная) часть тесно соприкасается с костной тканью.
В цитоплазме клетки, под ядрами, располагаются многочисленные лизосомы и вакуоли разной величины. Функциональная активность остеокласта проявляется следующим образом: в центральной (гофрированной) зоне основания клетки из цитоплазмы выделяются угольная кислота и протеолитические ферменты. Выделяющаяся угольная кислота вызывает деминерализацию костной ткани, а протеолитические ферменты разрушают органический матрикс межклеточного вещества. Фрагменты коллагеновых волокон фагоцитируются остеокластами и разрушаются внутриклеточно. Посредством этих механизмов происходит резорбция (разрушение) костной ткани и потому остеокласты обычно локализуются в углублениях костной ткани. После разрушения костной ткани за счет деятельности остеобластов, выселяющихся из соединительной ткани сосудов, происходит построение новой костной ткани.
Межклеточное вещество костной ткани состоит из основного вещества и волокон, в которых содержатся соли кальция. Волокна состоят из коллагена I типа и складываются в пучки, которые могут располагаться параллельно (упорядочено) или неупорядочено, на основании чего и строится гистологическая классификация костных тканей. Основное вещество костной ткани, как и других разновидностей соединительных тканей, состоит из гликозоаминогликанов и протеогликанов, однако химический состав этих веществ отличается. В частности в костной ткани содержится меньше хондроитинсерных кислот, но больше лимонной и других кислот, которые образуют комплексы с солями кальция. В процессе развития костной ткани вначале образуется органический матриксосновное вещество и коллагеновые (оссеиновые, коллаген II типа) волокна, а затем уже в них откладываются соли кальция (главным образом фосфорнокислые). Соли кальция образуют кристаллы гидроксиаппатита, откладывающиеся как в аморфном веществе, так и в волокнах, но небольшая часть солей откладывается аморфно. Обеспечивая прочность костей, фосфорнокислые соли кальция одновременно являются депо кальция и фосфора в организме. Поэтому костная ткань принимает участие в минеральном обмене.
При изучении костной ткани следует дифференцировать понятия костная ткань и кость.
3. Кость - это анатомический орган, основным структурным компонентом которого является костная ткань. Кость как орган состоит из следующих элементов:
Костная ткань;
Надкостница;
Костный мозг (красный, желтый);
Сосуды и нервы.
Надкостница (периост) окружает по периферии костную ткань (за исключением суставных поверхностей) и имеет строение сходное с надхрящницей. В надкостнице выделяют наружный фиброзный и внутренний клеточный или камбиальный слои. Во внутреннем слое содержатся остеобласты и остеокласты. В надкостнице локализуются выраженная сосудистая сеть, из которой мелкие сосуды через прободающие каналы проникают в костную ткань. Красный костный мозг рассматривается как самостоятельный орган и относится к органам кроветворения и иммуногенеза.
Костная ткань в сформированных костях представлена только пластинчатой формой, однако в разных костях, в разном участке одной кости она имеет разное строение. В плоских костях и эпифизах трубчатых костей костные пластинки образуют перекладины (трабекулы), составляющие губчатое вещество кости. В диафизах трубчатых костей пластинки прилежат друг к другу и образуют компактное вещество. Однако и в компактном веществе одни пластинки образуют остеоны, другие пластинки являются общими.
Строение диафиза трубчатой кости
На поперечном срезе диафиза трубчатой кости различают следующие слои:
Надкостница (периост);
Наружный слой общих или генеральных пластин;
Слой остеонов;
Внутренний слой общих или генеральных пластин;
Внутренняя фиброзная пластинкаэндост.
Наружные общие пластинки располагаются под надкостницей в несколько слоев, не образуя однако полные кольца. Между пластинками располагаются в лакунах остеоциты. Через наружные пластинки проходят прободающие каналы, через которые из надкостницы в костную ткань проникают прободающие волокна и сосуды. С помощью прободающих сосудов в костной ткани обеспечивается трофика, а прободающие волокна связывают надкостницу с костной тканью.
Слой остеонов состоит из двух компонентов: остеонов и вставочных пластин между ними. Остеон - является структурной единицей компактного вещества трубчатой кости. Каждый остеон состоит из:
5-20 концентрически наслоенных пластин;
Канала остеона, в котором проходят сосуды (артериолы, капилляры, венулы).
Между каналами соседних остеонов имеются анастомозы. Остеоны составляют основную массу костной ткани диафиза трубчатой кости. Они располагаются продольно по трубчатой кости соответственно силовым и гравитационным линиям и обеспечивают выполнение опорной функции. При изменении направления силовых линий в результате перелома или искривления костей остеоны не несущие нагрузку разрушаются остеокластами. Однако такие остеоны разрушаются не полностью, а часть костных пластин остеона по его длине сохраняется и такие оставшиеся части остеонов называются вставочными пластинками. На протяжении постнатального онтогенеза постоянно происходит перестройка костной ткани - одни остеоны разрушаются (резорбируются), другие образуются и потому всегда между остеонами находятся вставочные пластины, как остатки предшествующих остеонов.
Внутренний слой общих пластинок имеет строение аналогичное наружному, но он менее выражен, а в области перехода диафиза в эпифизы общие пластинки продолжаются в трабекулы.
Эндост - тонкая соединительно-тканная пластинка, выстилающая полость канала диафиза. Слои в эндосте четко не выражены, но среди клеточных элементов содержатся остеобласты и остеокласты.
Костная ткань представляет собой удивительное единство белковой основы и минерального субстрата, взаимно проникающих друг в друга. Белковая основа кости составляет 30%, минеральная субстанция – 60%, вода – 10%. Минеральный компонент костной ткани содержит от 1050 до 1200 г кальция, от 450 до 500 г фосфора, от 5 до 8 г магния. В костной ткани содержится фосфата кальция 85%, карбоната кальция 10%, фосфата магния 1,5%, фторида кальция 0,3%, различных микроэлементов 0,001%. Среди этих микроэлементов хлор, алюминий, бор, фтор, медь, марганец, серебро, свинец, стронций, барий, кадмий, кобальт, железо, цинк, титан, кремний и другие. Микроэлементы играют решающую роль в вегетативных процессах, протекающих в костной ткани. Например, медь активирует ферменты, вырабатываемые остеобластами, марганец ускоряет деятельность щелочной фосфотазы, цинк способствует работе ферментов окисления.
Костная ткань – это особый тип соединительной ткани, также состоящий из клеток и межклеточного вещества. К клеткам костной ткани относятся остеобласты, остеоциты, остеокласты. В отличие от других видов соединительной ткани кость характеризуется значительным содержанием межклеточного вещества и своеобразным его строением. Межклеточное вещество (костный матрикс) состоит из большого количества коллагеновых волокон (костный коллаген – оссеин), окруженных аморфным веществом (оссеомукоид). Оссеомукоид содержит гликопротеиды, мукополисахариды и большое количество солей кальция. Костная ткань благодаря своей прочности выполняет в организме функцию опоры и одновременно представляет собой депо минеральных солей.
Остеогенные клетки имеют мезенхимальную природу и образуются из полипотентных клеток, являющихся одновременно источником хрящевой и костной ткани.
В основном хрящи в организме развиваются в процессе внутриутробного развития и существуют временно, замещаясь в дальнейшем костью. Пока человек растет, сохраняются и функционируют хрящевые зоны роста. Огромное значение в функции опорно-двигательной системы играет гиалиновый хрящ, покрывающий концы костей, образующих суставы. Хрящевую ткань можно встретить в стенке трахеи, гортани, носу, в местах фиксации ребер к грудине.
Образующиеся в результате дифференцировки мезенхимальных клеток остеобласты отвечают за синтез новой кости. Одной из морфологических особенностей этих клеток является наличие у них длинных цитоплазматических отростков. Остеобласты синтезируют органический матрикс, который постепенно окружает клетки, как бы замуровывая их. В результате этого процесса образуются так называемые лакуны, содержащие костные клетки, которые теперь уже называются остеоцитами. Благодаря отросткам клетки соединяются друг с другом. Окруженные костным матриксом и соединенные между собой цитоплазматические отростки образуют систему костных канальцев. Остеокласты представляют собой группу клеток, отвечающих за резорбцию кости.
Остеогенные клетки расположены на костной поверхности в составе двух слоев: 1) периоста, покрывающего наружную поверхность кости и 2) эндоста, который выстилает внутренние поверхности всех полостей кости. Периост, в свою очередь, имеет два слоя: 1) наружный волокнистый и 2) внутренний остеогенный. Именно глубокий слой надкостницы принимает активное участие в остеогенезе. Надкостница содержит кровеносные сосуды, входящие в кость и выходящие из нее.
В процессе развития и роста костная ткань претерпевает определенные морфологические изменения. Выделяют два типа костной ткани: незрелую (грубоволокнистую) и зрелую (пластинчатую) костную ткань. Незрелая кость обычно встречается в организме человека в период эмбриогенеза, а также на ранних стадиях образования костной мозоли после перелома. Для незрелой кости характерно большее количество клеток. Межклеточное вещество содержит больше протеогликанов, гликопротеидов и кальция. Расположение волокон в костном матриксе напоминает сетку. Отсюда второе название этого типа кости – сетчатая. Рост кости в длину происходит за счет эпифизарных хрящевых ростковых пластинок. В толщину кость увеличивается в результате постепенного аппозиционного роста костной ткани снаружи и резорбции внутренней части костного вещества.
После рождения незрелая костная ткань постепенно замещается зрелой, которая уже представлена двумя видами: губчатой и компактной. Из губчатой ткани состоят кости запястья и предплюсны, тела позвонков, метафизы длинных трубчатых костей. Из компактной костной ткани образованы диафизы трубчатых костей.
Процесс образования костной ткани проходит вблизи мелких сосудов, так как клетки костной ткани нуждаются в питании. Образование костной ткани начинается с образованием костных трабекул, так называемых костных столбиков. Костные трабекулы состоят из остеобластов, которые располагаются по периферии, в центре находится межклеточное вещество кости, в некоторых участках которого могут отмечаться остеоциты. Постепенно развиваясь, трабекулы соединяются между собой и образуют разветвленную сеть. Такая анастомозирующая сеть костных трабекул называется губчатой костью. Характерной чертой этого вида костной ткани также является наличие расположенных между трабекулами полостей, заполненных соединительной тканью и кровеносными сосудами.
Для компактной кости характерно наличие главным образом костной ткани. Структурной единицей компактной кости является остеон или гаверсова система (по имени впервые описавшего ее Гаверса). Остеон представляет собой скопления соединенных между собой костными канальцами остеоцитов и органического матрикса, которые окружают один или два мелких сосуда. Канал, содержащий капилляр в центре остеона также получил название гаверсова. Размеры остеона в основном не превышают 0,4 мм. Остеоциты компактной кости располагаются концентрически по отношению к капилляру, что способствует беспрепятственному поступлению к ним тканевой жидкости от кровеносного сосуда, обеспечивающего их питание. Диаметр остеона ограничен расстоянием, на котором способны работать системы костных канальцев. Расстояние от клеток до центральных кровеносных сосудов не превышает обычно 0,1-0,2 мм. А число концентрических пластинок, окружающих гаверсов канал, не превышает пяти-шести. Пространства между гаверсовыми системами заполнены интерстициальными костными пластинками, именно поэтому поверхность компактной кости гладкая, а не бугристая.
Сосудистая сеть костной ткани представляет собой сложную систему, которая находиться в тесной связи с кровеносной системой окружающих мягких тканей. Кровоснабжение кости осуществляется из трех источников: 1) питающие артерии и вены; 2) сосуды метафиза; 3) сосуды надкостницы. Питающие артерии в количестве двух – трех проникают в кость на уровне верхней и средней третей диафиза через так называемые питающие отверстия и образуют медуллярную кровеносную сеть. Исключение составляет большеберцовая кость, имеющая только одну артерию, которая попадает в диафиз на уровне его верхней трети. Питающие артерии разветвляются по системе гаверсовых каналов и составляют почти 50 % массы кости. Сосуды метафиза принимают участие в кровоснабжении эпиметафизов трубчатых костей. Сосуды надкостницы проникают в кость по так называемым костным каналам Фолькмана и анастомозируют с сосудами гаверсовых систем. Экспериментально доказано, что сосуды надкостницы играют большую роль в полноценном венозном оттоке из кости, так как значительно более тонкая, чем артерия, питающая вена самостоятельно не смогла бы справиться с этой задачей. В настоящее время общепризнанно, что в кровоснабжении внутренних двух третей кортикального слоя в первую очередь принимают участие питающие артерии, а наружную треть дополнительно снабжают кровью сосуды надкостницы.
В течение всей жизни от момента начала эмбриогенеза до гибели организма костная ткань постоянно подвергается перестройке. В начале это связано с ростом и развитием организма. После окончания роста продолжается постоянная внутренняя перестройка, которая заключается в постепенной резорбции части костного вещества и замене его новой костью. Это объясняется тем, что гаверсовы системы компактной кости и трабекулы губчатой кости не сохраняются в течение всей жизни. Костная ткань, как и многие другие ткани в человеческом организме, должна все время постоянно обновляться. Ежегодно обновляется 2-4% костной ткани. До 20-30 летнего возраста происходит интенсивное накопление костной ткани. С 30 до 40 лет наступает период равновесия между процессами резорбции и восстановления. После 40 лет минеральная плотность костной ткани постепенно снижается.
Зубы располагаются в костных лунках - отдельных ячейках альвеолярных отростков верхней и нижней челюстей. Костная ткань - разновидность соединительной ткани, развивающаяся из мезодермы и состоящая из клеток, межклеточного неминерализованного органического матрикса (остеоид) и основного минерализованного межклеточного вещества.
5.1. ОРГАНИЗАЦИЯ И СТРОЕНИЕ КОСТНОЙ ТКАНИ АЛЬВЕОЛЯРНЫХ ОТРОСТКОВ
Поверхность кости альвеолярного отростка покрыта надкостницей (периост ), образованной преимущественно плотной волокнистой соединительной тканью, в которой различают 2 слоя: наружный - волокнистый и внутренний - остеогенный, содержащий остеобласты. Из остеогенного слоя надкостницы в кость проходят сосуды и нервы. Толстые пучки прободающих коллагеновых волокон связывают кость с надкостницей. Надкостница осуществляет не только трофическую функцию, но и участвует в росте и регенерации кости. Вследствие этого костная ткань альвеолярных отростков обладает высокой регенеративной способностью не только в физиологических условиях, при ортодонтических воздействиях, но и после повреждения (переломы).
Минерализованный матрикс организован в трабекулы - структурно-функциональные единицы губчатой костной ткани. В лакунах минерализованного матрикса и по поверхности трабекул располагаются клетки костной ткани - остеоциты, остеобласты, остеокласты.
В организме постоянно происходят процессы обновления костной ткани путём сопряженного по времени костеобразования и рассасы- вания (резорбция) кости. В этих процессах активно участвуют различные клетки костной ткани.
Клеточный состав костной ткани
Клетки занимают всего лишь 1-5% общего объёма костной ткани скелета взрослого человека. Различают 4 типа клеток костной ткани.
Мезенхимальные недифференцированные клетки кости находятся главным образом в составе внутреннего слоя надкостницы, покрывающей поверхность кости снаружи - периоста, а также в составе эндоста, выстилающего контуры всех внутренних полостей кости, внутренние поверхности кости. Их называют выстилающими , или контурными , клетками. Из этих клеток могут образовываться новые клетки кости - остеобласты и остеокласты. В соответствии с этой их функцией их также называют остеогенными клетками.
Остеобласты - клетки, находящиеся в зонах костеобразования на внешних и внутренних поверхностях кости. Остеобласты содержат достаточно большое количество гликогена и глюкозы. С возрастом это количество уменьшается в 2-3 раза. Синтез АТФ на 60% связан с реакциями гликолиза. По мере старения остеобластов реакции гликолиза активируются. В клетках протекают реакции цитратного цикла, и наибольшей активностью обладает цитратсинтаза. Синтезируемый цитрат используется в дальнейшем на связывание Ca 2+ , необходимого для процессов минерализации. Поскольку функцией остеобластов является создание органического межклеточного матрикса кости, эти клетки содержат большое количество РНК, необходимых для синтеза белков. Остеобласты активно синтезируют и выделяют во внеклеточное пространство значительное количество глицерофосфолипидов, которые способны связывать Ca 2+ и участвовать в процессах минерализации. Клетки сообщаются между собой через десмосомы, которые позволяют проходить Ca 2+ и цАМФ. Остеобласты синтезируют и выделяют в окружающую среду фибриллы коллагена, протеогликаны и гликозаминогликаны. Они также обеспечивают непрерывный рост кристаллов гидроксиапатитов и выступают в качестве посредников при связывании минеральных кристаллов с белковой матрицей. По мере старения остеобласты превращаются в остеоциты.
Остеоциты - древовидные клетки костной ткани, включенные в органический межклеточный матрикс, которые контактируют друг с другом через отростки. Остеоциты взаимодействуют и с другими клетками костной ткани: остеокластами и остеобластами, а также с мезенхимальными клетками кости.
Остеокласты - клетки, выполняющие функцию разрушения кости; образуются из макрофагов. Они осуществляют непрерывный управляемый процесс реконструкции и обновления костной ткани, обеспечивая необходимый рост и развитие скелета, структуру, прочность и упругость костей.
Межклеточное и основное вещество костной ткани
Межклеточное вещество представлено органическим межклеточным матриксом, построенным из коллагеновых волокон (90-95%) и основным минерализованным веществом (5-10%). Коллагеновые волокна в основном расположены параллельно направлению уровня наиболее вероятных механических нагрузок на кость и обеспечивают упругость и эластичность кости.
Основное вещество межклеточного матрикса состоит главным образом из внеклеточной жидкости, гликопротеинов и протеогликанов, участвующих в перемещении и распределении неорганических ионов. Минеральные вещества, размещённые в составе основного вещества в органическом матриксе кости представлены кристаллами, главным образом гидроксиапатитом Ca 10 (PO 4) 6 (OH) 2 . Соотношение кальций/фосфор в норме составляет 1,3-2,0. Кроме того, в кости обнаружены ионы Mg 2+ , Na + , K + , SO 4 2- , HCO 3- , гидроксильные и другие ионы, которые могут принимать участие в образовании кристаллов. Минерализация кости связана с особенностями гликопротеинов костной ткани и активностью остеобластов.
Основными белками внеклеточного матрикса костной ткани являются коллагеновые белки I типа, которые составляют около 90% органического матрикса кости. Наряду с коллагеном I типа присутствуют следы других типов коллагена, таких как V, XI, XII. Не исключено, что эти типы коллагена принадлежат другим тканям, которые и находятся в костной ткани, но не входят в состав костного матрикса. Например, коллаген V типа обычно обнаруживается в сосудах, которые пронизывают кость. Коллаген XI типа находится в хрящевой ткани и может соответствовать остаткам кальцифицированного хряща. Источником коллагена XII типа могут быть «заготовки» коллагеновых фибрилл. В костной ткани коллаген I типа содержит производные моносахаридов, имеет меньшее количество поперечных связей, чем в других видах соединительной ткани, и эти связи формируются посредством аллизина. Ещё одним возможным отличием является то, что N-концевой пропептид коллагена I типа фосфорилирован и этот пептид частично сохраняется в минерализованном матриксе.
В костной ткани содержится около 10% неколлагеновых белков. Они представлены гликопротеинами и протеогликанами (рис. 5.1).
Из общего количества неколлагеновых белков 10% приходится на долю протеогликанов. Вначале синтезируется большой хондроитин-
Рис. 5.1. Содержание неколлагеновых белков в межклеточном матриксе костной ткани [по Gehron R. P., 1992].
содержащий протеогликан, который по мере формирования костной ткани разрушается и замещается двумя малыми протеогликанами: декорином и бигликаном. Малые протеогликаны внедряются в мине- рализованный матрикс. Декорин и бигликан активируют процессы дифференцировки и пролиферации клеток, а также вовлечены в регуляцию отложения минералов, морфологию кристалла и объединение элементов органического матрикса. Первым синтезируется бигликан, содержащий дерматансульфат; он влияет на процессы клеточной пролиферации. В фазу минерализации появляется бигликан, связаный с хондроитинсульфатом. Декорин синтезируется позднее, чем бигликан, в стадию отложения белков для формирования межклеточного матрикса; он остаётся и в фазе минерализации. Предполагают, что декорин «отшлифовывает» молекулы коллагена и регулирует диаметр фибрилл. В ходе формирования кости оба белка продуцируются остеобластами, но когда эти клетки становятся остеоцитами, они синтезируют только бигликан.
Из костного матрикса в небольших количествах были выделены и другие типы малых протеогликанов, которые выступают в качестве
рецепторов и облегчают связывание факторов роста с клеткой. Эти типы молекул находятся в мембране или прикрепляются к клеточной мембране посредством фосфоинозитоловых связей.
В костной ткани также присутствует гиалуроновая кислота. Вероятно, она играет важную роль в морфогенезе этой ткани.
Помимо протеогликанов в кости определяется большое количество разнообразных белков, относящихся к гликопротеинам (табл. 5.1).
Как правило, эти белки синтезируются остеобластами и способны связывать фосфаты или кальций; таким образом они принимают участие в формировании минерализованного матрикса. Связываясь с клет- ками, коллагенами и протеогликанами, они обеспечивают образование надмолекулярных комплексов матрикса костной ткани (рис. 5.2).
В остеоиде присутствуют протеогликаны: фибромодулин, бигликан, декорин, коллагеновые белки и морфогенетический белок кости. В минерализованном матриксе замурованы остеоциты, которые связаны с коллагенами. На коллагенах фиксированы гидроксиапатиты, остеокальцин, остеоадерин. В минерализованном межклеточном

Рис. 5.2. Участие различных белков в образовании матрикса костной ткани.
Таблица 5.1
Неколлагеновые белки костной ткани
Белок | Свойства и функции |
Остеонектин | Гликофосфопротеин, способный связывать Са 2+ |
Щелочная фосфатаза | Отщепляет фосфат от органических соединений при щелочных значениях pH среды |
Тромбоспондин | Белок с мол. массой 145 кДа, состоящий из трех идентичных субъединиц, связанных друг с другом дисульфидными связями. Каждая субъединица имеет несколько различных доменов, которые придают белку способность связываться с другими белками костного матрикса - гепарансодержащими протеогликанами, фибронектином, ламинином, коллагеном I и V типов и остеонектином. В N-кон- цевой области тромбоспондина содержится последовательность аминокислот, обеспечивающая прикрепление клеток. На связывание тромбоспондина с рецепторами на поверхности клетки влияет кон- центрация Ca 2+ . В костной ткани тромбоспондин синтезируется остеобластами |
Фибронектин | Связывается с поверхностью клеток, фибрином, гепарином, бактериями, коллагеном. В костной ткани фибронектин синтезируется на ранних стадиях остеогенеза и сохраняется в минерализован- ном матриксе |
Остеопонтин | Гликофосфопротеин, содержащий N- и О-связанные олигосахариды; участвует в адгезии клеток |
Костный кислый гликопротеин-75 | Белок с мол. массой 75 кДа, содержит сиаловые кислоты и остатки фосфата. Способен связывать ионы Са 2+ , присущ кости, дентину и хрящевой ростковой пластинке. Ингибирует процессы резорбции костной ткани |
Костный сиалопротеин | Адгезивный гликопротеин, содержащий до 50% углеводов |
Матриксный Gla-белок | Белок, содержащий 5 остатков 7-карбоксиглутами- новой кислоты; способен связываться с гидроксиапатитом. Появляется на ранних стадиях развития костной ткани; белок обнаружен также в лёгких, сердце, почках, хряще |
матриксе остеоадерин связывается с остеонектином, а остеокальцин с коллагеном. Морфогенетический белок кости располагается в приграничной зоне между минерализованным и неминерализованным матриксом. Остеопонтин регулирует активность остеокластов.
Свойства и функции белков костной ткани представлены в табл. 5.1.
5.2. ФИЗИОЛОГИЧЕСКАЯ РЕГЕНЕРАЦИЯ КОСТНОЙ ТКАНИ
В процессе жизнедеятельности кость постоянно обновляется, то есть разрушается и восстанавливается. При этом в ней происходят два противоположно направленных процесса - резорбция и восстановление. Соотношение этих процессов называется ремоделированием костной ткани.
Известно, что каждые 30 лет костная ткань изменяется почти полностью. В норме кость «растет» до 20-летнего возраста, достигая пика костной массы. В этот период прирост костной массы составляет до 8% в год. Далее до 30-35-летнего возраста идет период более или менее устойчивого состояния. Затем начинается естественное постепенное снижение костной массы, составляющее обычно не более 0,3-0,5% в год. После наступления менопаузы у женщин отмечается максимальная скорость потери костной ткани, которая достигает 2-5% в год и продолжается в таком темпе до 60-70 лет. В итоге женщины теряют от 30 до 50% костной ткани. У мужчин эти потери обычно составляют 15-30%.
Процесс ремоделирования костной ткани происходит в несколько этапов (рис. 5.3). На первом этапе участок костной ткани, подле-

Рис. 5.3. Стадии ремоделирования костной ткани [по Martin R.B., 2000, с изменениями].
жащий резорбции запускают остеоциты. Для активации процесса необходимо участие паратиреоидного гормона, инсулиноподобного фактора роста, интерлейкинов-1 и -6, простагландинов, кальцитриола, фактора некроза опухоли. Тормозится этот этап ремоделирования эстрогенами. На данном этапе поверхностные контурные клетки изменяют свою форму, превращаясь при этом из плоских округлых клеток в кубические.
Остеобласты и Т-лимфоциты секретируют лиганды рецепторов активатора фактора нуклеации каппа В (RANKL) и до определённого момента молекулы RANKL могут оставаться связанными с поверхностью остеобластов или стромальных клеток.
Из стволовой клетки костного мозга образуются предшественники остеокластов. Они имеют мембранные рецепторы, называемые рецепторами активатора фактора нуклеации каппа В (RANK). На следующем этапе RANK-лиганды (RANKL) связываются с RANK- рецепторами, что сопровождается слиянием нескольких предшественников остеокластов в одну крупную структуру и формируются зрелые многоядерные остеокласты.
Образующийся активный остеокласт создаёт на своей поверхности гофрированный край и зрелые остеокласты начинают резорбировать
костную ткань (рис. 5.4). На стороне прилегания остеокласта к разрушаемой поверхности различают две зоны. Первая зона - наиболее обширная, называемая щеточной каемкой, или гофрированным краем. Гофрированный край - это скрученная спиралью мембрана с множественными цитоплазматическими складками, которые обращены в сторону резорбции на костной поверхности. Через мембрану остеокласта освобождаются лизосомы, содержащие большое количество гидролитических ферментов (катепсины К, D, B, кислая фосфатаза, эстераза, гликозидазы и др). В свою очередь, катепсин К активирует матриксную металлопротеиназу-9, которая участвует в деградации коллагена и протеогликанов межклеточного матрикса. В этот период в остеокластах растёт активность карбоангидразы. Ионы НСО 3 - обме- ниваются на Cl - , которые накапливаются в гофрированном крае; туда же переносятся ионы H + . Секреция H + осуществляется за счёт очень активной в остеокластах Н + /К + -АТФазы. Развивающийся ацидоз способствует активации лизосомных ферментов и способствует разруше- нию минерального компонента.
Вторая зона окружает первую и как бы герметизирует область действия гидролитических ферментов. Она свободна от органелл и назы-

Рис. 5.4. Активация преостеокласта RANKL и формирование активным остеобластом гофрированной каймы, приводящей к резорбции костной ткани [по Edwards P. A., 2005, с изменениями].
вается чистой зоной, поэтому костная резорбция происходит только под гофрированным краем в замкнутом пространстве.
На стадии образования остеокластов из предшественников процесс может блокироваться белком остеопротегерином, который, свободно перемещаясь, способен связывать RANKL и таким образом предотвращать взаимодействие RANKL с RANK-рецепторами (см. рис. 5.4). Остеопротегерин - гликопротеин с мол. массой 60-120 кДа, относящийся к семейству рецепторов ФНО. Ингибируя связывание RANK с RANK-лигандом, остеопротегерин тем самым подавляет мобилизацию, пролиферацию и активацию остеокластов, поэтому увеличение синтеза RANKL приводит к резорбции костной ткани и, следовательно, к потере костной массы.
Характер ремоделирования костной ткани во многом определяется балансом между продукцией RANKL и остеопротегерина. Недифференцированные стромальные клетки костного мозга в большей степени синтезируют RANKL и в меньшей степени остеопротегерин. Возникающий дисбаланс системы RANKL/остеопротегерин при увеличении RANKL приводит к резорбции кости. Данное явление наблюдается при постменопаузальном остеопорозе, болезни Педжета, костных потерях при метастазах рака и ревматоидном артрите.
Зрелые остеокласты начинают активно поглощать кость, а завершают разрушение органической матрицы межклеточного вещества кости макрофаги. Резорбция длится около двух недель. Затем остеокласты в соответствии с генетической программой умирают. Апоптоз остеокластов может задерживаться при недостатке эстрогенов. На последнем этапе в зону разрушения прибывают плюрипотентные стволовые клетки, которые дифференцируются в остеобласты. В дальнейшем остеобласты синтезируют и минерализуют матрикс в соответствии с новыми условиями статической и динамической нагрузки на кость.
Существует большое число факторов, стимулирующих развитие и функции остеобластов (рис. 5.5). Вовлечение в процесс перестройки кости остеобластов стимулируется различными факторами роста - ТФР-(3, морфогенетическим белком кости, инсулиноподобным фактором роста, фактором роста фибробластов, тромбоцитов, колониестимулирующим и гормонами - паратирином, кальцитриолом, а также связывающим фактором ядра α-1 и тормозится белком лептином. Лептин - белок с мол. массой 16 кДа образуется преимущественно в адипоцитах; своё действие реализует через повышение синтеза цитокинов, факторов роста эпителия и кератиноцитов.

Рис. 5.5. Ремоделирование костной ткани.
Активные секретирующие остеобласты создают слои остеоида - неминерализованного матрикса кости и медленно восполняют полость резорбции. При этом они секретируют не только различные факторы роста, а также белки межклеточного матрикса - остеопонтин, остеокальцин и другие. Когда образующийся остеоид достигает диаметра 6?10 -6 м, он начинает минерализоваться. Скорость процесса минерализации зависит от содержания кальция, фосфора и ряда микроэлементов. Процесс минерализации управляется остеобластами и тормозится пирофосфатом.
Образование кристаллов минерального остова кости индуцирует коллаген. Формирование минеральной кристаллической решётки начинается в зоне, находящейся между коллагеновыми фибриллами. Затем они, в свою очередь, становятся центрами для отложения в пространстве между коллагеновыми волокнами (рис. 5.6).
Формирование кости происходит только в непосредственной близости от остеобластов, причём минерализация начинается в хряще,

Рис. 5.6. Отложение кристаллов гидроксиапатита на коллагеновых волокнах.
который состоит из коллагена, находящегося в протеогликановом матриксе. Протеогликаны повышают растяжимость коллагеновой сети. В зоне кальцификации происходит разрушение комплексов белок-полисахарид в результате гидролиза белкового матрикса лизосомальными ферментами клеток кости. По мере роста кристаллы вытесняют не только протеогликаны, но и воду. Плотная, полностью минерализованная кость, практически обезвожена; коллаген составляет 20% массы и 40% объема такой ткани; остальное приходится на долю минеральной части.
Начало минерализации характеризуется усиленным поглощением остеобластами молекул O 2 , активацией окислительно-восстановительных процессов и окислительного фосфорилирования. В митохондриях накапливаются ионы Ca 2+ и PO 4 3- . Начинается синтез коллагеновых и неколлагеновых белков, которые затем после посттрансляционной модификации секретируются из клетки. Формируются различные везикулы, в составе которых переносится коллаген, протеогликаны и гликопротеины. От остеобластов отпочковываются особые образования, называемые матриксными пузырьками, или мембранными везикулами. Они содержат в большой концентрации ионы Ca 2+ , которая превышает в 25-50 раз содержание их в остеобластах, а также глицерофосфолипиды и ферменты - щелочную фосфатазу, пирофосфатазу,
аденозинтрифосфатазу и аденозинмонофосфатазу. Ионы Ca 2+ в мембранных везикулах связаны преимущественно с отрицательно заряженым фосфатидилсерином. В межклеточном матриксе мембранные везикулы разрушаются с освобождением ионов Ca 2+ , пирофосфатов, органических соединений, связанных с остатками фосфорной кислоты. Присутствующие в мембранных везикулах фосфогидролазы, и в первую очередь щелочная фосфатаза, отщепляют фосфат от органических соединений, а пирофосфат гидролизуется пирофосфатазой; ионы Ca 2+ соединяются с PO 4 3- , что приводит к появлению аморфного фосфата кальция.
Одновременно происходит частичное разрушение протеогликанов, связанных с коллагеном I типа. Освобождающиеся фрагменты протеогликанов, заряженные отрицательно, начинают связывать ионы Ca 2+ . Некоторое число ионов Ca 2+ и PO 4 3 образуют пары и триплеты, которые связываются с коллагеновыми и неколлагеновыми белками, формирующими матрицу, что сопровождается образованием кластеров, или ядер. Из белков костной ткани наиболее активно связывают ионы Ca 2+ и PO 4 3 остеонектин и матриксные Gla-белки. Коллаген костной ткани связывает ионы РО 4 3 через ε-аминогруппу лизина с образованием фосфоамидной связи.
На образовавшемся ядре возникают спиралевидые структуры, рост которых идет по обычному принципу добавления новых ионов. Шаг такой спирали равен высоте одной структурной единицы кристалла. Формирование одного кристалла приводит к появлению других кристаллов; этот процесс называется эпитаксисом, или эпитаксической нуклеацией.
Рост кристалла высоко чувствителен к присутствию других ионов и молекул, которые ингибируют кристаллизацию. Концентрация этих молекул может быть небольшой, и они оказывают влияние не только на скорость, но на форму и направление роста кристаллов. Предполагают, что такие соединения адсорбируются на поверхности кристалла и тормозят адсорбцию других ионов. Такими веществами являются, например, гексаметафосфат натрия, который тормозит преципитацию карбоната кальция. Пирофосфаты, полифосфаты и полифосфонаты также тормозят рост кристаллов гидроксиапатита.
Через несколько месяцев, после того как полость резорбции восполнится костной тканью, плотность новой кости увеличивается. Остеобласты начинают превращаться в контурные клетки, которые участвуют в непрерывном выведении кальция из кости. Некоторые
из остеобластов превращаются в остеоциты. Остеоциты остаются в кости; они связаны друг с другом длинными клеточными отростками и способны воспринимать механические воздействия на кость.
По мере дифференцировки и старения клеток меняется характер и интенсивность обменных процессов. С возрастом в 2-3 раза уменьшается количество гликогена; освобождающаяся глюкоза в молодых клетках на 60% используется в реакциях анаэробного гликолиза, а в старых на 85%. Синтезированные молекулы АТФ необходимы для жизнеобеспечения и минерализации костных клеток. В остеоцитах остаются лишь следы гликогена, и основным поставщиком молекул АТФ является только гликолиз, за счёт которого поддерживается постоянство органического и минерального состава в уже минерализованных отделах костной ткани.
5.3. РЕГУЛЯЦИЯ МЕТАБОЛИЗМА В КОСТНОЙ ТКАНИ
Ремоделирование костной ткани регулируется системными (гормоны) и местными факторами, которые обеспечивают взаимодейс- твие между остеобластами и остеокластами (табл. 5.2).
Системные факторы
Образование кости в известной степени зависит от числа и активности остеобластов. На процесс образования остеобластов влияют
Таблица 5.2
Факторы, регулирующие процессы ремоделирования кости

соматотропин (гормон роста), эстрогены, 24,25(ОН) 2 D 3 , которые стимулируют деление остеобластов и превращение преостеобластов в остеобласты. Глюкокортикоиды, напротив, подавляют деление остеобластов.
Паратирин (паратгормон) синтезируется в паращитовидных железах. Молекула паратирина состоит из одной полипептидной цепи, содержащей 84 аминокислотных остатков. Синтез паратирина стимулирует адреналин, поэтому в условиях острого и хронического стресса количество этого гормона увеличивается. Паратирины активирует пролиферацию клеток-предшественников остеобластов, продлевает время их полужизни и ингибирует апоптоз остеобластов. В костной ткани рецепторы для паратирина присутствуют в мембранах остеобластов и остеоцитов. Остеокласты лишены рецепторов для данного гормона. Гормон связывается с рецепторами остеобластов и активирует аденилатциклазу, что сопровождается увеличением количества 3" 5" цАМФ. Такое повышение содержания цАМФ способствует интенсивному поступлению ионов Ca 2+ из внеклеточной жидкости. Поступивший кальций образует комплекс с кальмодулином и далее происходит активация кальцийзависимой протеинкиназы с последующим фос- форилированием белков. Связываясь с остеобластами, паратирин вызывает синтез остеокласт-активирующего фактора - RANKL, способного связываться с преостеокластами.
Введение больших доз паратирина приводит к гибели остеобластов и остеоцитов, что сопровождается увеличением зоны резорбции, повышением уровня кальция и фосфатов в крови и моче с одновре- менным повышением экскреции гидроксипролина вследствие разрушения коллагеновых белков.
Рецепторы к паратирину располагаются и в почечных канальцах. В проксимальных отделах почечных канальцев гормон ингибирует реабсорбцию фосфата и стимулирует образование 1,25(ОН) 2 D 3 . В дистальных отделах почечных канальцев паратирин усиливает реабсорбцию Ca 2+ . Таким образом, паратирин обеспечивает повышение уровня кальция и снижение фосфатов в плазме крови.
Паротин - гликопротеин, выделяемый околоушными и поднижне- челюстными слюнными железами. Белок состоит из α-, β -, и γ-субъединиц. Активным началом паротина является γ-субъединица, которая оказывает влияние на мезенхимные ткани - хрящ, трубчатые кости, дентин зуба. Паротин усиливает пролиферацию хондрогенных клеток, стимулирует синтез нуклеиновых кислот и ДНК в одонтобластах, про-
цессы минерализации дентина и костей. Эти процессы сопровождаются понижением содержания кальция и глюкозы в плазме крови.
Кальцитонин - полипептид, состоящий из 32 аминокислотных остат- ков. Секретируется парафолликулярными К-клетками щитовидной железы или С-клетками паращитовидных желёз в виде высокомолекулярного белка-предшественника. Секреция кальцитонина возрастает при увеличении концентрации ионов Са 2+ и уменьшается при понижении концентрации ионов Са 2+ в крови. Она также зависит от уровня эстрогенов. При недостатке эстрогенов секреция кальцитонина снижается. Это вызывает усиление мобилизации кальция в костной ткани и способствует развитию остеопороза. Кальцитонин связывается с специфическими рецепторами остеокластов и клеток почечных канальцев, что сопровождается активацией аденилатциклазы и повышением образования цАМФ. Кальцитонин влияет на транспорт ионов Ca 2+ через клеточные мембраны. Он стимулирует поглощение ионов Ca 2+ митохондриями и тем самым задерживает отток ионов Ca 2+ из клетки. Этот зависит от количества АТФ и соотношения ионов Na + и K + в клетке. Кальцитонин угнетает распад коллагена, что проявляется уменьшением экскреции с мочой гидроксипролина. В клетках почечных канальцев кальцитонин ингибирует гидроксилирование 25(ОН)D 3 .
Таким образом, кальцитонин подавляет активность остеокластов и ингибирует освобождение ионов Ca 2+ из костной ткани, а также уменьшает реабсорбцию ионов Ca 2+ в почках. В результате тормозится резорбция костной ткани, стимулируются процессы минерализации, что проявляется понижением уровня кальция и фосфора в плазме крови.
Йодсодержащие гормоны щитовидной железы - тироксин (Т4) и трийодтиронин (Т3) обеспечивают оптимальный рост костной ткани. Тиреоидные гормоны способны стимулировать секрецию гормонов роста. Они повышают как синтез мРНК инсулиноподобного фактора роста 1 (ИФР-1), так и продукцию самого ИФР-1 в печени. При гипертиреозе подавляется дифференцировка остеогенных клеток и синтез белка в этих клетках, снижается активность щелочной фосфатазы. За счёт усиленной секреции остеокальцина активируется хемотаксис остеокластов, что ведёт к резорбции костной ткани.
Половые стероидные гормоны участвуют в процессах ремоделирования костной ткани. Воздействие эстрогенов на костную ткань проявляется в активации остеобластов (прямое и опосредованное действие), угнетении остеокластов. Они также способствуют всасыванию ионов Ca 2+ в желудочно-кишечном тракте и его отложению в костной ткани.
Женские половые гормоны стимулируют продукцию кальцитонина щитовидной железой и снижают чувствительность костной ткани к паратирину. Они также вытесняют на конкурентной основе кортикостероиды из их рецепторов в костной ткани. Андрогены, оказывая анаболическое действие на костную ткань, стимулируют биосинтез белка в остеобластах, а также ароматизируются в жировой ткани в эстрогены.
В условиях дефицита половых стероидов, который имеет место в менопаузе, процессы костной резорбции начинают преобладать над процессами ремоделирования костной ткани, что и приводит к раз- витию остеопении и остеопороза.
Глюкокортикоиды синтезируются в коре надпочечников. Основной глюкокортикоид человека - кортизол. Глюкокортикоиды скоординировано действуют на разные ткани и разные процессы - как анаболические, так и катаболические. В костной ткани кортизол тормозит синтез коллагена I типа, некоторых неколлагеновых белков, протеогликанов и остеопонтина. Глюкокортикоиды также уменьшают количество тучных клеток, являющихся местом образования гиа- луроновой кислоты. Под влиянием глюкокортикоидов ускоряется распад белков. Глюкокортикоиды подавляют всасывание ионов Ca 2+ в кишечнике, что сопровождается снижением его в сыворотке крови. Это понижение приводит к выбросу паратирина, который стимулирует образование остеокластов и резорбцию кости (рис. 5.7). Кроме того, кортизол в мышцах и костях стимулирует распад белков, что также нарушает формирование костной ткани. В конечном итоге действия глюкокортикоидов приводят к убыли костной ткани.
Витамин D 3 (холекальциферол) поступает с пищей, а также образуется из предшественника 7-дегидрохолестерола под влиянием ультрафиолетовых лучей. В печени холекальциферол превращается в 25(ОН)D 3 , а в почках происходит дальнейшее гидроксилирование 25(ОН)D 3 и образуются 2 гидроксилированных метаболита - 1,25(ОН) 2 D 3 и 24,25(ОН) 2 D 3 . Метаболиты витамина D 3 регулируют хондрогенез и остеогенез уже в процессе эмбрионального развития. В отсутствии витамина D 3 невозможна минерализация органического матрикса, при этом не образуется сосудистая сеть, а метафизарная кость не способна сформироваться должным образом. 1,25(ОН) 2 D 3 связывается с хондробластами, находящимся в активном состоянии, а 24,25(ОН) 2 D 3 - с клетками в состоянии покоя. 1,25(ОН) 2 D 3 регулирует зоны роста через образование комплекса с ядерным рецептором для этого витамина. Также показано, что 1,25(ОН) 2 D 3 способен связы-
Рис. 5.7. Схема влияния глюкокортикоидов на обменные процессы, приводящие к убыли костной ткани
ваться с мембранно-ядерным рецептором, что приводит к активации фосфолипазы С и образованию инозитол-3-фосфата. Кроме того, образующийся комплекс активируется фосфолипазой А 2 . Из осво- бождающейся арахидоновой кислоты синтезируется простагландин Е 2 , который также влияет на ответ хондробластов при их связывании с 1,25(ОН) 2 D 3 . Напротив, после связывания 24,25(ОН) 2 D 3 со своим мембранно-связывающимся рецептором, активируется фосфолипаза С, а затем протеинкиназа С.
В хрящевой зоне роста эпифизов костной ткани 24,25(ОН) 2 D 3 стимулирует дифференцировку и пролиферацию прехондробластов, которые содержат специфические рецепторы к данному метаболиту. Метаболиты витамина D 3 оказывают влияние на формирование и функциональное состояние височно-нижнечелюстного сустава.
Витамин А . При недостатке и избыточном поступлении витамина А в организм детей нарушается рост костей и происходит их деформация. Вероятно, эти явления обусловлены деполимеризацией и гидролизом хондроитинсульфата, входящего в состав хряща.

Витамин С . При недостатке аскорбиновой кислоты в мезенхемаль- ных клетках не происходит гидроксилирование остатков лизина и пролина, что приводит к нарушению образования зрелого коллагена. Образующийся незрелый коллаген не способен связывать ионы Ca 2+ и таким образом нарушаются процессы минерализации.
Витамин Е . При дефиците витамина Е в печени не образуется 25(ОН)D 3 - предшественник активных форм витамина D 3 . Дефицит витамина Е также может привести к снижению уровня магния в костной ткани.
Локальные факторы
Простагландины ускоряют выход ионов Ca 2+ из кости. Экзогенные простагландины увеличивают генерацию остеокластов, которые раз- рушают кость. Оказывают катаболическое воздействие на обмен белков в костной ткани и ингибирует их синтез.
Лактоферрин - железосодержащий гликопротеин, в физиологической концентрации стимулирует пролиферацию и дифференцировку остеобластов, а также ингибирует остеокластогенез. Митогенный эффект лактоферрина на остеобластоподобные клетки осуществляется через специфические рецепторы. Образовавшийся комплекс путём эндоцитоза поступает в клетку, и лактоферрин фосфорилирует митоген - активирующие протеинкиназы. Таким образом, лактоферрин выполняет роль фактора роста кости и её здоровья. Может применяться в качестве анаболического фактора при остеопорозе.
Цитокины - низкомолекулярные полипептиды, обусловливающие взаимодействие клеток иммунной системы. Они обеспечивают ответную реакцию на внедрение чужеродных тел, иммунное повреждение, а также воспаления, репарации и регенерации. Они представлены пятью большими группами белков, одной из которых являются интерлейкины.
Интерлейкины (ИЛ ) - белки (от ИЛ-1 до ИЛ-18), синтезируемые в основном Т-клетками лимфоцитов, а также мононуклеарными фагоцитами. Функции ИЛ связаны с активностью других физиологически активных пептидов и гормонов. В физиологической концентрации подавляют рост, дифференцировку и продолжительность жизни клеток. Cнижают продукцию коллагеназы, адгезию эндотелиальных клеток к нейтрофилам и эозинофилам, продукцию NO и, как следс- твие, наблюдается уменьшение деградации хрящевой ткани и резорбция кости.
Процесс резорбции костной ткани может активироваться при ацидозе и большими количествами интегринов, ИЛ и витамина A, но тормозится эстрогенами, кальцитонином, интерфероном и морфогенетическим белком кости.
Маркёры метаболизма костной ткани
Биохимические маркёры дают информацию о патогенезе заболеваний скелета и о фазах ремоделирования костной ткани. Различают биохимические маркёры формирования и резорбции кости, характе- ризующие функции остеобластов и остеокластов.
Прогностическая значимость определения маркёров метаболизма костной ткани:
Проведённый скрининг с использованием данных маркёров позволяет определить пациентов с высоким риском развития остеопороза; высокие уровни маркёров резорбции костей могут быть связаны с
увеличением риска переломов; повышение уровня маркёров метаболизма костной ткани у пациентов с остеопорозом более чем в 3 раза по сравнению с показателями нормы предполагает иную костную патологию, включая злокачественную; маркёры резорбции могут быть использованы в качестве дополнительных критериев при решении вопроса о назначении специальной терапии при лечении костной патологии. Маркёры резорбции кости . Во время обновления костной ткани коллаген I типа, который составляет более 90% органического матрикса кости и синтезируется непосредственно в костях, деградирует, а небольшие пептидные фрагменты попадают в кровь или выделяются почками. Продукции деградации коллагена можно определять как в моче, так и в сыворотке крови. Эти маркёры можно использовать при терапии препаратами, снижающими резорбцию костей, у пациентов с болезнями, связанными с нарушениями метаболизма костной ткани. В качестве критериев резорбции костной ткани выступают продукты деградации коллагена I типа: N- и С-телопептиды и тартрат-резистентная кислая фосфатаза. При первичном остеопорозе и болезни Педжета происходит отчетливое повышение С-концевого телопептида коллагена I типа и количество этого маркёра увеличивается в сыворотке крови в 2 раза.
Распад коллагена - единственный источник свободного гидроксипролина в организме. Преобладающая часть гидроксипролина
катаболизируется, а часть выделяется с мочой, главным образом, в составе небольших пептидов (ди- и трипептидов). Поэтому содержание гидроксипролина в крови и моче отражает баланс скорости катаболизма коллагена. У взрослого человека в сутки экскретируется 15-50 мг гидроксипролина, в молодом возрасте до 200 мг, а при некоторых болезнях, связанных с поражением коллагена, например: гиперпаратироидизме, болезни Педжета и наследственной гипергидроксипролинемии, причиной которой является дефект фермента гидроксипролиноксидазы, количество в крови и выделяемого с мочой гидроксипролина увеличивается.
Остекласты секретируют тартрат-резистентную кислую фосфатазу. При возрастании активности остеокластов происходит увеличение содержания тартрат-резистентной кислой фосфатазы и она попадает в повышенном количестве в кровоток. В плазме крови активность этого фермента возрастает при болезни Педжета, онкологических заболеваниях с метастазами в кость. Определение активности этого фермента особенно полезно при мониторинге лечения остеопороза и онкологических заболеваний, сопровождающихся поражением костной ткани.
Маркёры формирования кости . Формирование костной ткани оценивают по количеству остеокальцина, костного изофермента щелочной фосфатазы и остеопротегерина. Измерение количества сывороточного остеокальцина позволяет определять риск развития остеопороза у женщин, проводить мониторинг костного метаболизма во время менопаузы и гормональной заместительной терапии. Рахит у детей раннего возраста сопровождается снижением в крови содержания остеокальцина и степень снижения его концентрации зависит от выраженности рахитического процесса. У больных с гиперкортицизмом и пациентов, получающих преднизолон, значительно снижено содержание остеокальцина в крови, что отражает подавление процессов костеобразования.
Изофермент щелочной фосфатазы присутствует на клеточной поверхности остеобластов. При увеличенном синтезе фермента клетками костной ткани повышается его количество в плазме крови, поэтому определение активности щелочной фосфатазы, особенно костного изофермента, является информативным показателем костного ремоделирования.
Остеопротегерин выступает в качестве рецептора ФНО. Связываясь с преостеокластами, он ингибирует мобилизацию, пролиферацию и активацию остеокластов.
5.4. РЕАКЦИЯ КОСТНОЙ ТКАНИ НА ДЕНТАЛЬНЫЕ
ИМПЛАНТАТЫ
При различных формах адентии альтернативой съёмному протезированию являются внутрикостные дентальные имплантаты. Реакцию костной ткани на имплантат можно рассматривать как частный случай репаративной регенерации.
Различают три вида соединения дентальных имплантатов с костной тканью:
Прямое приживление - остеоинтеграция;
Фиброзно-оссальная интеграция, когда вокруг дентального имплантата образуется слой фиброзной ткани толщиной около 100 мкм;
Периодонтальное соединение (самый редкий вид), образующееся в случае периодонтального связочно-подобного сращения с периимплантационными коллагеновыми волокнами или (в некоторых случаях) цементирование внутрикостного дентального имплантата.
Считают, что в процессе остеоинтеграции после постановки дентальных имплантатов образуется тонкая зона из протеогликанов, которая лишена коллагена. Зона склеивания дентального имплантата с костью обеспечивается двойным слоем протеогликанов, включающим молекулы декорина.
При фиброзно-оссальной интеграции в соединении имплантата с костной тканью также участвуют многочисленные компоненты внеклеточного матрикса. За устойчивость имплантата в его капсуле отвечают коллагены I и III типа, а фибронектин играет основную роль в связывании элементов соединительной ткани с имплантатами.
Однако через какой-то период времени под действием механической нагрузки растёт активность коллагеназы, катепсина К и кислой фосфатазы. Это приводит к убыли костной ткани в периимплантационной области и происходит дезинтеграция дентального имплантата. Ранняя дезинтеграция внутрикостных дентальных имплантатов происходит на фоне сниженного количества в кости фибронектина, Gla-белка, тканевого ингибитора матриксных металлопротеиназ (ТИМП-1).
Развитие костей зависит от двух механизмов: внутримембранного костного формирования и эндохондрального формирования. Для восстановления костей используются те же механизмы, но они определяются факторами окружающей среды. Рост костей и его поддержание особенно зависят от сосудистой системы и от межклеточной связи через лакунарную каналикулярную систему .Состав костной ткани:
- костные клетки, или остеоциты;основное вещество;коллагеновые волокна;цементирующая субстанция;разнообразные соли.
- ретикулярная;пластинчатая.
а) Ретикулярная костная ткань
Это результат трансформации соединительной ткани в костную. Такие кости мы наблюдаем в основном во время развития, а также у взрослых около краниальных швов.б) Пластинчатая костная ткань (рис. 62)
Она составляет основную массу костей во взрослом организме и имеет очень четкое расслоение из-за основного вещества в форме пластин, чередующихся со слоями остеоцитов, расположенных концентрически вокруг гаверсовых каналов: эта структура формирует остеон. Между остеонами находятся интерстициальные гаверсовых каналов пластины — гаверсовы каналы, которые связываются в конечные костные каналы Волкманна (Volkmann). Рис. 62. Схематическое изображение двух остеоцитов и части системы Структура и расположение остеонов зависят от нагрузок на кость — мы находим ту же схему, что и в фасциях.Развитие костной ткани осуществляется благодаря остеобластам — специфическим клеткам, происходящим от ме-зенхиматозных клеток, родоначальников всех тканей.Они секретируют остеоидную межклеточную субстанцию, изначально состоящую из мягкого основного вещества и коллагеновых волокон.Электрическая стимуляция вызывает синтез внеклеточного матрикса, кальцификацию и образование кости. Электрические поля стимулируют клеточную дифференциацию и увеличивают число молекул, синтезируемых клетками . Внутренние биофизические силы будут способствовать костному росту в трех плоскостях пространства,тогда как внешние силы будут способствовать росту в функциональных направлениях. Кроме того, они могут лежать в основе различных патологий .2. Виды оссификации Различают два вида оссификации:- прямая (внутрисоединительная, или фиброзная);непрямая — энхондральная (путем замещения хряща).
а) Оссификация внутрисоединительная
Образование костной ткани идет от соединительной ткани. Вначале кость фиброзная, затем она трансформируется в пластинчатую. Этот тип оссификации встречается в:- костях свода черепа;костях лица;ключице.
6) Энхондральная оссификация
Есть предварительная необходимость представить отдельные части хрящевого скелета, состоящего из хондробластов (они разрушают хрящевую ткань и начинают формировать костную ткань из остеобластов).Различают два типа энхондральной оссификации:- энхондральная оссификация, идущая внутри хряща на уровне эпифизов;перихондральная оссификация — идет от перихондрия и ограничена областью диафиза.
- короткая кость — тесное прилегание;широкая кость - прилегание слабое;длинная кость - прилегание слабое на уровне диафизов и сильное на уровне эпифизов.
- прикреплении сухожилий и фасций к кости — что фиксирует их к кости;имплантации в кость нервов и сосудов, исходящих из периоста;проникновении в кость соединительных волокон, исходящих из периоста, составляющих волокна Шарпи (терминальная точка фасций).
а) Внутренняя поверхность
Имеет сосуды и нервные ветви, предназначенные для кости. Следом идет слой костномозговых клеток, участвующих в росте и уплотнении кости.б) Наружная поверхность
Связана с мышцами, сухожилиями, фасциями. Она находится в связи с кожей и отделена от нее фасцией или неплотной клеточной тканью (большеберцовая кость, скуловая кость).в) Структура
Надкостница состоит из фиброзной ткани, в ней различают два ложа:- наружный слой, сформированный из соединительной ткани с примесью эластических волокон;внутренний слой, сформированный из тех же элементов, но более тонких.
а) Межклеточная матрица
Она состоит из органической матрицы основного вещества и волокон минерализированного коллагена, а также минеральных солей.- Органическая матрица Органическая матрица состоит из многочисленных коллагеновых волокон. Были выявлены трубчатые внутрикостные фибриллы, которые являются продолжением фибрилл прикрепления сухожилия или фасции. Это волокна Шарли.Минеральные соли
б) Формирование и резорбция костной ткани
В течение всей жизни костная ткань является местом непрерывного обновления, где происходят конструктивные и деструктивные процессы.1) Формирование костной ткани Вначале происходит образование предкостного вещества остеобластами, которые секретируют и синтезируют гликопротеины, мукополисахариды и молекулы тропоколлагена.Затем происходит минерализация через:- отложение фосфорно-кальциевых солей;создание кристаллов гидроксиапатита.
- Остеокластическая резорбция, стимулируемая гормоном паращитовидной железы. Остеокласт секретирует ионы Н+, которые будут растворять минеральную субстанцию; окисленные гидролазы, полимеризируются в гликопротеины и мукополисахариды коллагеназы, атакующие коллаген;Резорбция периостеоцитарная: некоторые остеокласты имеют большую литическую активность и определяют деминерализацию и лизис окружающей костной ткани.
В состав скелета любого взрослого человека входит 206 различных костей, все они различны по строению и роли. На первый взгляд они кажутся твердыми, негибкими и безжизненными. Но это ошибочное впечатление, в них непрерывно происходят различные обменные процессы, разрушение и регенерация. Они, в совокупности с мышцами и связками, образуют особую систему, что носит название "костно-мышечная ткань", основная функция которой - опорно-двигательная. Она образована из нескольких видов особых клеток, которые различаются по структуре, функциональным особенностям и значению. О костных клетках, их строение и функциях далее и пойдет речь.
Строение костной ткани
Особенности пластинчатой костной ткани
Она образована костными пластинками, имеющими толщину 4-15 мкм. Они, в свою очередь, состоят их трех компонентов: остеоцитов, основного вещества и коллагеновых тонких волокон. Из этой ткани образованы все кости взрослого человека. Волокна коллагена первого типа лежат параллельно относительно друг друга и ориентированы в определенном направлении, у соседних же костных пластинок они направлены в противоположную сторону и перекрещиваются практически под прямым углом. Между ними находятся тела остеоцитов в лакунах. Такое строение костной ткани обеспечивает ей наибольшую прочность.
Губчатое вещество кости

Встречается также название "трабекулярное вещество". Если проводить аналогию, то структура сравнима с обычной губкой, построенной из костных пластинок с ячейками между ними. Расположены они упорядоченно, в соответствии с распределенной функциональной нагрузкой. Из губчатого вещества в основном построены эпифизы длинных костей, часть смешанных и плоских и все короткие. Видно, что в основном это легкие и в то же время прочные части скелета человека, которые испытывают нагрузку в различных направлениях. Функции костной ткани находятся в прямой взаимосвязи с ее строением, которое в данном случае обеспечивает большую площадь для метаболических процессов, осуществляемых на ней, придает высокую прочность в совокупности с небольшой массой.
Плотное (компактное) вещество кости: что это?
Из компактного вещества состоят диафизы трубчатых костей, кроме того, оно тонкой пластинкой покрывает их эпифизы снаружи. Его пронизывают узкие каналы, через них проходят нервные волокна и кровеносные сосуды. Некоторые из них располагаются параллельно костной поверхности (центральные или гаверсовы). Другие выходят на поверхность кости (питательные отверстия), через них внутрь проникают артерии и нервы, а наружу - вены. Центральный канал, в совокупности с окружающими его костными пластинками, образует так называемую гаверсову систему (остеон). Это основное содержимое компактного вещества и их рассматривают как его морфофункциональную единицу.
Остеон - структурная единица костной ткани

Второе его название - гаверсова система. Это совокупность костных пластинок, имеющих вид цилиндров вставленных друг в друга, пространство между ними заполняют остеоциты. В центре располагается гаверсов канал, через него проходят обеспечивающие обмен веществ в костных клетках кровеносные сосуды. Между соседними структурными единицами есть вставочные (интерстициальные) пластинки. По сути, они являются остатками остеонов, существовавших ранее и разрушившихся в тот момент, когда костная ткань претерпевала перестройку. Также существуют еще генеральные и окружающие пластинки, они образуют самый внутренний и наружный слой компактного вещества кости соответственно.
Надкостница: строение и значение
Исходя из названия, можно определить, что она покрывает кости снаружи. Прикрепляется она к ним с помощью коллагеновых волокон, собранных в толстые пучки, которые проникают и сплетаются с наружным слоем костных пластинок. Имеет два выраженных слоя:
- наружный (его образует плотная волокнистая, неоформленная соединительная ткань, в ней преобладают волокна, располагающиеся параллельно к поверхности кости);
- внутренний слой хорошо выражен у детей и менее заметен у взрослых (образован рыхлой волокнистой соединительной тканью, в которой есть веретенообразные плоские клетки - неактивные остеобласты и их предшественники).

Надкостница выполняет несколько важных функций. Во-первых, трофическую, то есть обеспечивает кость питанием, поскольку на поверхности содержит сосуды, которые проникают внутрь вместе с нервами через специальные питательные отверстия. Эти каналы питают костный мозг. Во-вторых, регенераторную. Она объясняется наличием остеогенных клеток, которые при стимуляции трансформируются в активные остеобласты, вырабатывающие матрикс и вызывающие наращивание костной ткани, обеспечивающие ее регенерацию. В-третьих, механическую или опорную функцию. То есть обеспечение механической связи кости с другими прикрепляющимися к ней структурами (сухожилиями, мышцами и связками).
Функции костной ткани
Среди основных функций можно перечислить следующие:
- Двигательная, опорная (биомеханическая).
- Защитная. Кости оберегают от повреждений головной мозг, сосуды и нервы, внутренние органы и т. д.
- Кроветворная: в костном мозге происходит гемо - и лимфопоэз.
- Метаболическая функция (участие в обмене веществ).
- Репараторная и регенераторная, заключающиеся в восстановлении и регенерации костной ткани.
- Морфобразующая роль.
- Костная ткань - это своеобразное депо минеральных веществ и ростовых факторов.